Inducción de estructuras callogénicas en explantes in vitro y ex vitro de Cinchona officinalis L
DOI:
https://doi.org/10.54753/blc.v16i1.2633Palabras clave:
Cinchona officinalis, desinfección, callogénesis, micropropagaciónResumen
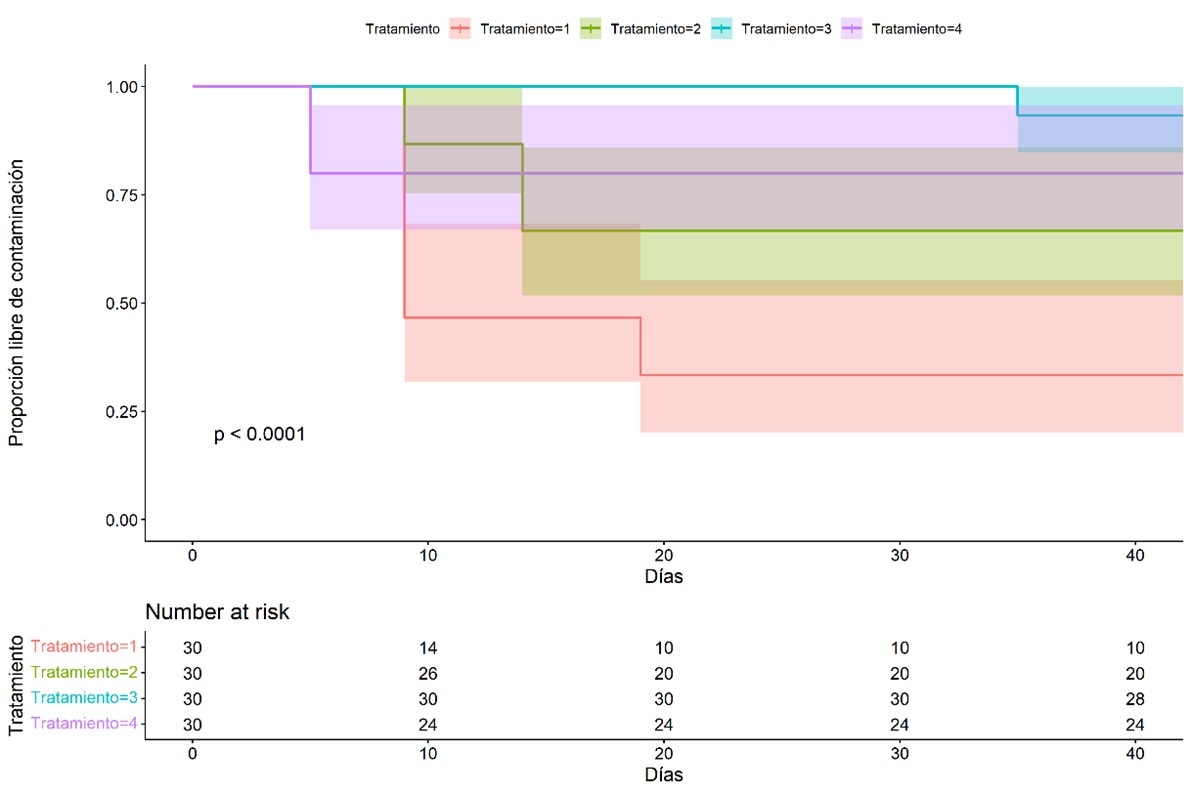
Cinchona officinalis L., especie emblemática del sur del Ecuador sobreexplotada históricamente y con baja capacidad de regeneración natural, fue objeto del presente estudio en donde se evaluó la desinfección de material vegetal ex vitro (invernadero) y, la interacción de auxinas y citoquininas para inducir estructuras callogénicas con material in vitro y ex vitro. En ambos casos se aplicó un diseño completamente al azar. En la primera fase se probó cuatro concentraciones de NaClO (10-15-20-25 % por 10 minutos), los resultados de mayor control de contaminación fueron con el T3 y T4 con 93 % y 80 % de eficiencia respectivamente, la fenolización del T3 fue del 80 %. En la segunda fase se evaluaron cinco tratamientos de ANA/KIN (0-10 mg L⁻¹ ANA + 0-0.5 mg L⁻¹ KIN) para la obtención de estructuras callogénicas, se inoculó explantes de 1 cm de nervadura central/hojas, se incubaron en oscuridad total por 90 días; los resultados mostraron ser superiores en T1-T4 (76-100 %) con relación al 13-33 % obtenido a partir de material ex vitro, la contaminación fue nula (excepto 7 % en T3) en in vitro, frente al 60-80 % en ex vitro, la rizogénesis en T3-T4 (46-70 raíces/callo in vitro vs. 28-33 ex vitro). La fenolización elevada (72 % in vitro, 92 % ex vitro), identificándose como barrera crítica. Se demostró que la combinación de NaClO al 20 %, antioxidantes y balance ANA/KIN (5-10 + 0,5 mg L⁻¹) en vitroplantas es eficiente para estimular la callogénesis y micropropagación de cinchona.Citas
Arbizu, C., Ferro-Mauricio, R., Chávez-Galarza, J., Guerrero-Abad, J., Vásquez, H., & Maicelo, J. L. (2021). The complete chloroplast genome of the national tree of Peru, quina (Cinchona officinalis L., Rubiaceae). Mitochondrial DNA Part B, 6(9), 2781-2783. https://doi.org/10.1080/23802359.2021.1969697
Armijos-González R, Pérez-Ruiz C (2016) In vitro germination and shoot proliferation of the threatened species Cinchona officinalis L (Rubiaceae). J Forestry Res 27(6):1229–1236. https://doi.org/10.1007/s11676-016-0272-8
Armijos-González, R., Ramón, P. & Cueva-Agila, A. Cinchona officinalis L. ex situ conservation by in vitro slow growth and cryopreservation techniques. Plant Cell Tiss Organ Cult 158, 6 (2024). https://doi.org/10.1007/s11240-024-02784-8
Azofeifa, Á. (2009). Problemas de oxidación y oscurecimiento de explantes cultivados in vitro. Agronomía mesoamericana, 20(1), 153-175. https://doi.org/10.15517/am.v20i1.4990
Bogado, F. A., Vera Bravo, C., Ayala, P. G., Sansberro, P. A., & Luna, C. V. (2016). Uso de distintos desinfectantes superficiales para el establecimiento in vitro de segmentos nodales de Grevillea robusta. Ciencias Agronómicas, 16(27), 11–16. https://ri.conicet.gov.ar/handle/11336/25301
Camacho, J. (2023). Formación de estructuras callogénicas en explantes obtenidos de vitroplantas de Cinchona officinalis L., en condiciones de fotoperíodo y oscuridad. [Tesis de pregrado, Universidad Nacional de Loja]. Repositorio Digital - Universidad Nacional de Loja. https://dspace.unl.edu.ec/jspui/handle/123456789/26058
Caraguay. K, Eras, V, González, D, et al. (2016). Potencial reproductivo y análisis de calidad de semillas de Cinchona officinalis L., provenientes de relictos boscosos en la Provincia de Loja – Ecuador. Rev. Investig. Altoandin. Vol. 18 Nro. 3: 271- 280. https://dialnet.unirioja.es/servlet/articulo?codigo=5645611
Castillo, A. (2004). Propagación de plantas por cultivo in vitro: una biotecnología que nos acompaña hace mucho tiempo. INIA, Investigadora, Unidad de Biotecnología. https://ainfo.inia.uy/digital/bitstream/item/410/1/111219220807102417.pdf
Cupueran, F, Barragán, O, Insuasti, J, Barrigas, D, y Soto, C (2021). Producción de plantas in vitro de quina (Cinchona officinalis): una revisión de plantas in vitro de quina (Cinchona officinalis): una revisión. Revista Biorrefinería Vol., 4 (4). https://cebaecuador.org/wp-content/uploads/2022/01/13.pdf
Díaz, G. (2012). Procesos morfogénicos in vitro de Cedro (Cedrela montana Mortiz ex Turcz.) Inducidos a partir de semillas, para propagación y conservación de germoplasma. [Tesis pregrado, Universidad Nacional de Loja]. Repositorio Digital - Universidad Nacional de Loja. https://dspace.unl.edu.ec/jspui/handle/123456789/5343
Díaz Lezcano, M. I., Rodas Ramírez, J. M., González Segnana, L. R., & Vera de Ortiz, M. (2020). Establecimiento in vitro de segmentos nodales de Handroanthus heptaphyllus de flores blancas. Biotecnología Vegetal, 20(3), 203-210. http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S2074-86472020000300203&lng=es&nrm=iso
Duque, J. P. (2010). Biotecnología. Netbiblo. https://bit.ly/3S1PWYG
Eras-Guamán, V., Moreno, J., Yaguana, M., Poma, R., y Paredes, D. (2019). Balance hormonal para la fase de brotación y enraizamiento in vitro de explantes de Cinchona officinalis L., provenientes de relictos boscosos de la provincia de Loja. Bosques Latitud Cero, 9(1), 58-68. https://revistas.unl.edu.ec/index.php/bosques/article/view/586
Eras-Guamán, V. H., Moreno-Serrano, J., Méndez-Montaño, K., Yaguana-Arévalo, M., y Angamarca, R. A. P. (2019). Procesos biotecnológicos para la formación de callos y estructuras de novo de Cinchona officinalis L. provenientes de relictos boscosos de la provincia de Loja. Bosques Latitud Cero, 9(2), 20-28. https://revistas.unl.edu.ec/index.php/bosques/article/view/682
Eras-Guamán, V. H., Moreno-Serrano, J., Yaguana-Arévalo, M., Poma Angamarca, R., y Guartanza-Loja, J. A. (2020). Inducción in vitro de estructuras callogénicas en Cinchona officinalis L. Bosques Latitud Cero, 10(1), 14–28. https://revistas.unl.edu.ec/index.php/bosques/article/view/714
Eras Guamán, V. H., Moreno Serrano, J. A., Yaguana Arévalo, M., Poma Angamarca, R. A., y Cueva Coronel, C. M. (2021). Inducción in vitro de raíces de Cinchona officinalis L., a partir de vitroplantas. Bosques Latitud Cero, 11(2), 43–52. https://revistas.unl.edu.ec/index.php/bosques/article/view/1006
Espinosa, A., Silva, J., Sariego, S., Cholo Masapanta, L., y Delgado, H. (2012). Efecto del tipo de explante y la concentración de ácido 2, 4-diclorofenoxiacético en la formación de callos en Morus alba L. Pastos y Forrajes, 35(4), 407-416. http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S0864-03942012000400006&lng=es&nrm=iso
García, D., Ocampo, M., y Mesa, N. (2015). Estandarización del protocolo de desinfección para la micropropagación de Aspidosperma polyneuron. Revista Colombiana de Biotecnología, 17(2), 76-84. https://doi.org/10.15446/rev.colomb.biote.v17n2.54277
Garmendia, A. (2005). El árbol de la quina (Cinchona spp.): distribución, caracterización de su hábitat y arquitectura. 187. bit.ly/3NNKohS
González Valdiviezo, K., Eras Guamán, V. H., Moreno Serrano, J., Minchala Patiño, J., Yaguana Arévalo, M., y Valarezo Ortega, C. (2018). Procesos biotecnológicos para la inducción de callos a partir de vitroplantas de Cinchona officinalis L., a nivel de laboratorio en la provincia de Loja, Ecuador. Tzhoecoen, 10(2), 299-312. https://dialnet.unirioja.es/servlet/articulo?codigo=8152310
Gu, M., Li, Y., Jiang, H., Zhang, S., Que, Q., Chen, X., & Zhou, W. (2022). Efficient In Vitro Sterilization and Propagation from Stem Segment Explants of Cnidoscolus aconitifolius (Mill.) I.M. Johnst, a Multipurpose Woody Plant. Plants, 11(15), 1937. https://doi.org/10.3390/plants11151937
Hernández, Y., y González, M. (2010). Efectos de la contaminación microbiana y oxidación fenólica en el establecimiento in vitro de frutales perennes. Instituto Nacional de Ciencias Agropecuarias (INCA), 31, 88–100. https://doi.org/0258-5936
Levitus, G., Echenique, V., Rubinstein, C., Hopp, E., & Mroginski, L. (2010). Biotecnología y mejoramiento vegetal II. Instituto Nacional de Tecnología Agropecuaria, Argentina, 258.
Liu et al. (2024) Liu, C., Fan, H., Zhang, J., Wu, J., Zhou, M., Cao, F., Tao, G., & Zhou, X. (2024). Combating browning: mechanisms and management strategies in vitro culture of economic woody plants. Forestry Research, 4, e032. https://doi.org/10.48130/forres-0024-0026
López Correa, J. E., y Botero, L. R. (2015). Cultivo in vitro de la especie forestal amenazada Peltogyne purpurea Pittier. Universidad Nacional de la Plata. http://sedici.unlp.edu.ar/handle/10915/58549
López, N. (2016). Evaluación del paisaje y recursos escénicos después de 350 años de explotación de la “cascarilla" o “quina” Cinchona officinalis L. (Rubiaceae) en el sector Cajanuma-Rumishitana, Ecuador. Arnaldoa, 23(2). https://doi.org/10.22497/668
Martínez, M., Hernández, C., y Restrepo, L. (2007). Estandarización de un protocolo para la obtención de callos friables de borojó (Borojoa patinoi Cuatr.) fase I. Revista Colombiana de Biotecnología. ISSN: 0123-3475. https://www.redalyc.org/pdf/776/77690205.pdf
Medina, J., y Catarí, E. (2022). Caracterización química de la corteza del árbol de la Quina (Cinchona officinalis) para su consideración como materia prima lignocelulósica. Ciencia en Revolución, 8(23), 36-59. https://cienciaenrevolucion.com.ve/index.php/cienciaenrevolucion/article/view/60
Murashige T., Skoog F. (1962). A revised medium for rapid growth and bioassays with tobacco tissue culture. Physiologia Plantarum. 15 (3): 473-497. https://onlinelibrary.wiley.com/doi/10.1111/j.1399-3054.1962.tb08052.x
Oran, S., Althaher, A., & Mubarak, M. (2022). Cinchona officinalis (cinchona Tree) and Corylus avellana (common hazel). In Herbs, Shrubs, and Trees of Potential Medicinal Benefits (pp. 377-394). CRC Press. DOI:10.1201/9781003205067-19
Parveen, S., Maurya, N., Meena, A. y Luqman, S. (2024). Cinconina: un agente farmacológico versátil derivado de alcaloides naturales de la quina. Temas actuales en química medicinal, 24 (4), 343-363. 10.2174/0115680266270796231109171808
Ramírez, L., Granados, J., y Carreño, N. (2014). Evaluación del efecto de tratamientos de desinfección con hipoclorito de sodio sobre segmentos nodales de Guadua angustifolia Kunth para el establecimiento del cultivo in vitro. Dialnet. 5(1), 1-15. https://dialnet.unirioja.es/servlet/articulo?codigo=5344976
Regalado, A., Paccha, E., Álvarez, O., y Montaño, T. (2020). Comportamiento de las concentraciones de PM10 en la ciudad de Loja-Ecuador y su relación con variables meteorológicas. Journal of Science and Research, 5(1), 137-148. https://revistas.utb.edu.ec/index.php/sr/article/view/755
Rodríguez-Layza, J., Gonzales-Arteaga, J. J., Romero-Rivas, L. C., y Párraga-Quintanilla, A. (2021). Establecimiento in vitro de café var. caturra roja a partir de microesquejes. Ciencia Latina Revista Científica Multidisciplinar, 5(5), 8132-8148. https://doi.org/10.37811/cl_rcm.v5i5.894
Rodríguez Beraud, M. M., Latsague Vidal, M. I., Chacón Fuentes, M. A., & Astorga Brevis, P. K. (2014). Inducción in vitro de callogénesis y organogénesis indirecta a partir de explantes de cotiledón, hipocótilo y hoja en Ugni molinae. Bosque (Valdivia), 35(1), 111-118. http://dx.doi.org/10.4067/S0717-92002014000100011
Romero, J. (2015). Rasgos morfológicos de frutos, semillas y embriones de Cinchona officinalis L. (Rubiaceae) en el sur del Ecuador. Revista Ecuatoriana de Medicina y Ciencias Biológicas, 36(1-2), 27-35. https://dialnet.unirioja.es/servlet/articulo?codigo=6369414
Sánchez-Calvo, L., y Alvarenga-Venutolo, S. (2015). Callogénesis y establecimiento del cultivo de células en suspensión de Uncaria tomentosa (Willd.) DC (uña de gato). Revista Tecnología en Marcha, 28(1), 105-120. https://www.scielo.sa.cr/scielo.php?script=sci_arttext&pid=S0379-39822015000100105&lng=en&nrm=iso
Sánchez, R. y Luberli, J. (2023). Efecto de tres dosis y dos reguladores de crecimiento en la propagación in vitro de Cinchona officinalis L. (Rubiaceae)-Cajamarca. http://hdl.handle.net/20.500.14074/6217
Sánchez-Santillan, T., Meléndez-Mori, JB, Morales-Rojas, E., Chichipe-Puscan, AK, Oliva-Cruz, SM y Huaman-Vela, MH (2021). Multiplicación clonal del árbol de quina (Cinchona officinalis L.): una alternativa para conservar el árbol nacional del Perú. 33(3) 215-222. https://dialnet.unirioja.es/servlet/articulo?codigo=8135617
Serrano, J. A. M., Ruíz, C. P., Fierro, I. M., & Fierro, J. M. (2019). Effect of culture medium on morphogenic processes in vitro in Cinchona officinalis L. Revista de la Facultad de Ciencias Agrarias UNCuyo, 51(1), 55-68. https://revistas.uncu.edu.ar/ojs3/index.php/RFCA/article/view/2337
Setiawan et al. (2020) Setiawan, R. B., Rahmah, M., Trisnia, H., Chaniago, I., Syukriani, L., Yunita, R., & Jamsari, J. (2020). Embryogenic callus induction of coffee [Coffea arabica L.] on several plant growth regulator concentration and incubation temperature. IOP Conference Series: Earth and Environmental Science, 497, 012012. https://doi.org/10.1088/1755-1315/497/1/012012
Sharry, S. (2015). Plantas de probeta. Editorial de la Universidad Nacional de La Plata (EDULP). ISBN: 978-950-34-1254-1 https://doi.org/10.35537/10915/46738
Publicado
Cómo citar
Número
Sección
Licencia
Derechos de autor 2025 Andr´és Armijos Montaño, Marcia Manchay Loaiza , Magaly Yaguana Arévalo

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial-CompartirIgual 4.0.
Esta obra se publica bajo la licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional (CC BY-NC-SA 4.0). Esto significa que los usuarios pueden copiar, distribuir y adaptar el contenido, siempre que se otorgue el crédito adecuado a los autores y a la revista. No se permite el uso comercial del material. Además, cualquier obra derivada debe distribuirse bajo la misma licencia. Esta licencia garantiza el acceso abierto al conocimiento, promoviendo la difusión y reutilización de los trabajos publicados sin fines de lucro, respetando la autoría y asegurando la libre circulación del contenido en términos equitativos.